
Na esteira de flexibilizações decorrentes do coronavírus, a liberação emergencial da telemedicina começa a gerar impactos relevantes para o avanço da Saúde Digital no Brasil. A Portaria MS 467/2020, que regula a prática em caráter excepcional e temporário, também autorizou expressamente a emissão de atestados e receitas médicas por meio eletrônico, sendo esta última sujeita a regras específicas e requisitos formais, quais sejam:
- A utilização de certificados e chaves emitidos pela Infraestrutura de Chaves Públicas Brasileira (ICP-Brasil);
- O uso de dados associados à assinatura do médico de tal modo que qualquer modificação posterior possa ser detectável;
- Inclusão de identificação do médico, associação ou anexo de dados em formato eletrônico e admissão como válida pela pessoa a quem for oposto o documento.
Prescrição Digitalizada x Prescrição Digital
É importante esclarecer que a prescrição digitalizada é tão somente uma fotocópia ou cópia digitalizada de uma receita emitida e assinada de forma manual pelo médico. Este formato é autorizado apenas para medicamentos sujeitos à prescrição em receita simples, ou ainda, isentos de prescrição médica.
Já a prescrição eletrônica ou digital conta, necessariamente, como uma com assinatura digital certificada pelo sistema de Infraestrutura de Chaves Públicas Brasileira (ICP-Brasil), podendo ser encaminhada ao paciente ou seu representante legal via SMS, email ou QR Code. Sua aplicabilidade é limitada aos medicamentos de controle especial e antimicrobianos, conforme estabelecido pela Agência Nacional de Vigilância Sanitária (Anvisa) através da Nota Técnica 31/2020.
Neste caso, antes de dispensar o medicamento, a farmácia pode confirmar a validade da prescrição eletrônica através de um verificador de documentos disponibilizado pelo governo federal.
Em complemento, o Conselho Federal de Medicina (CFM), o Conselho Federal de Farmácia (CFF) e o Instituto Nacional de Tecnologia da Informação (ITI) desenvolveram um projeto de prescrição eletrônica, que pretende viabilizar o trâmite seguros de interações entre médicos, farmacêuticos e pacientes, através da disponibilização gratuita dos seguintes modelos de documentos médicos (clique para abrir):
- Receituário Simples
- Receituário de Controle Especial
- Receituário Antimicrobianos
- Atestado Médico
- Relatório Médico
- Solicitação de Exames
Assinatura certificada pela ICP-Brasil
Criada através da Medida Provisória nº 2.200-2, de 24 de agosto de 2011, a Infraestrutura de Chaves Pública Brasileira é uma cadeia hierárquica de confiança que estabelece padrões técnicos para emissão de certificados digitais, bem como para validade jurídica de documentos assinados eletronicamente.
Com a assinatura eletrônica garantem-se a autoria, integridade e autenticidade do documento, já que a tecnologia da ICP-Brasil criptografa o seu conteúdo, evitando alterações. Este mecanismo também garante que o responsável pela assinatura esteja ciente e de acordo com o seu conteúdo.
Através do Parecer CFM nº 30/2014, o Conselho Federal de Medicina reconheceu a validade de documentos digitais, estabelecendo que arquivos contendo uma certificação digital em conformidade com a ICP-Brasil deverão ser considerados como tendo sido assinados pela pessoa ou instituição para a qual o respectivo certificado digital foi emitido.
Mais recentemente, em decorrência da Emergência de Saúde Pública de Importância Nacional (Espin) da Covid-19, o Comitê Gestor da Infraestrutura de Chaves Públicas Brasileira publicou a Resolução nº 170, de 24 de abril de 2020, que estabelece procedimentos para emissão de certificados digitais por meio de videoconferência, em caráter extraordinário enquanto durar o período de pandemia.
Neste formato, os certificados digitais possuirão validade de no máximo um ano e não poderão ser renovados, estando dispensada a coleta de impressões digitais do responsável.
Alterações legislativas Medida Provisória 983/20
Através da Medida Provisória nº 983/20, foi alterada a redação da Lei nº 5.991/73, dispõe sobre o controle sanitário do comércio de drogas, medicamentos, insumos farmacêuticos e correlatos. A nova redação exclui a necessidade de receitas serem escritas em tinta, além de estabelecer que receitas em meio eletrônico somente serão válidas se contiverem a assinatura eletrônica do profissional e atenderem requisitos estabelecidos pela Anvisa ou Ministério da Saúde.
Em complemento, a MP determina que documentos subscritos por profissionais de saúde e relacionados à sua área de atuação são válidos para todos os fins quando assinados através das seguintes modalidades:
- Assinatura eletrônica avançada: que está associada ao signatário de maneira unívoca e utiliza dados cujo signatário pode, com elevado nível de confiança, operar sob o seu controle exclusivo, bem como está relacionada aos dados a ela associados de tal modo que qualquer modificação posterior é detectável;
- Assinatura eletrônica qualificada: que utiliza certificado digital reconhecido pela ICP-Brasil.
O texto da MP 983/20 possui validade de 60 dias, prorrogáveis por igual período. Embora os efeitos jurídicos de uma medida provisória sejam imediatos, seu texto depende de apreciação pelas casas do Congresso Nacional (Câmara e Senado) para se converter definitivamente em lei ordinária. Se não for apreciada em até 45 dias, contados da sua publicação, a MP entra em regime de urgência, sobrestando todas as demais deliberações legislativas da casa em que estiver tramitando.
Dispensação de medicamentos durante a pandemia
Em decorrência das medidas de distanciamento social, a Anvisa publicou a Resolução da Diretoria Colegiada nº 357, de 24 de março de 2020, que flexibiliza as quantidades máximas de medicamentos sujeitos a controle especial. A regra é válida, em princípio, por um período de seis meses. Confira abaixo as quantidades atualmente permitidas:
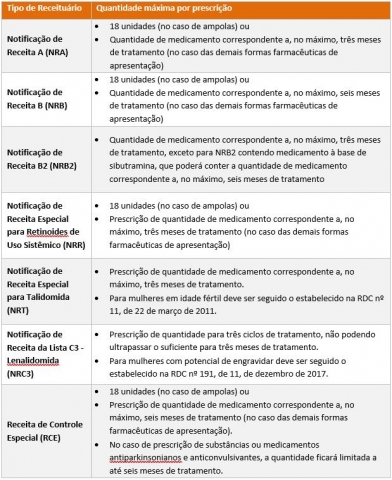
A Resolução ainda permite a entrega remota de medicamentos sujeitos a controle especial, desde que atendidos os seguintes requisitos pelo estabelecimento dispensador:
- Retenção da notificação de receita ou da receita de controle especial;
- Oferecimento de assistência farmacêutica remota;
- Controle e o monitoramento das dispensações de medicamentos entregues remotamente através de um formulário de registro de entrega em domicílio;
- Buscar a notificação de receita ou a receita de controle especial no local onde se encontra o paciente e, somente após a conferência do farmacêutico da regularidade da prescrição, proceder à entrega do medicamento;
- Disponibilização dos registros para fins de acompanhamento do paciente e fiscalização pela autoridade sanitária competente.
É importante notar que, em linha com o estabelecido sobre boas práticas farmacêuticas na Resolução de Diretoria Colegiada nº 44, de 17 de agosto de 2009, a nova regulação também proíbe expressamente a compra e a venda de medicamentos sujeitos ao controle especial através da internet.
*Ana Candida Sammarco, Marcelo Mansur Haddad e Maria Fernanda de A. Prado e Silva são advogados do escritório Mattos Filho.



Add new comment